1. Phenol là gì?
- Phenol là một hợp chất hữu cơ thơm có công thứ hóa học là C6H5OH. Cấu tạo của nó là sự kết hợp giữa một nhóm phenyl ( −C6H5) liên kết với một nhóm hydroxyl (-OH). Đây là một hóa chất có tính độc tố cao và khả năng gây bỏng nặng nếu vô tình tiếp xúc với da. Chính vì đặc tính này, Phenol tuyệt đối bị cấm sử dụng trong ngành thực phẩm.
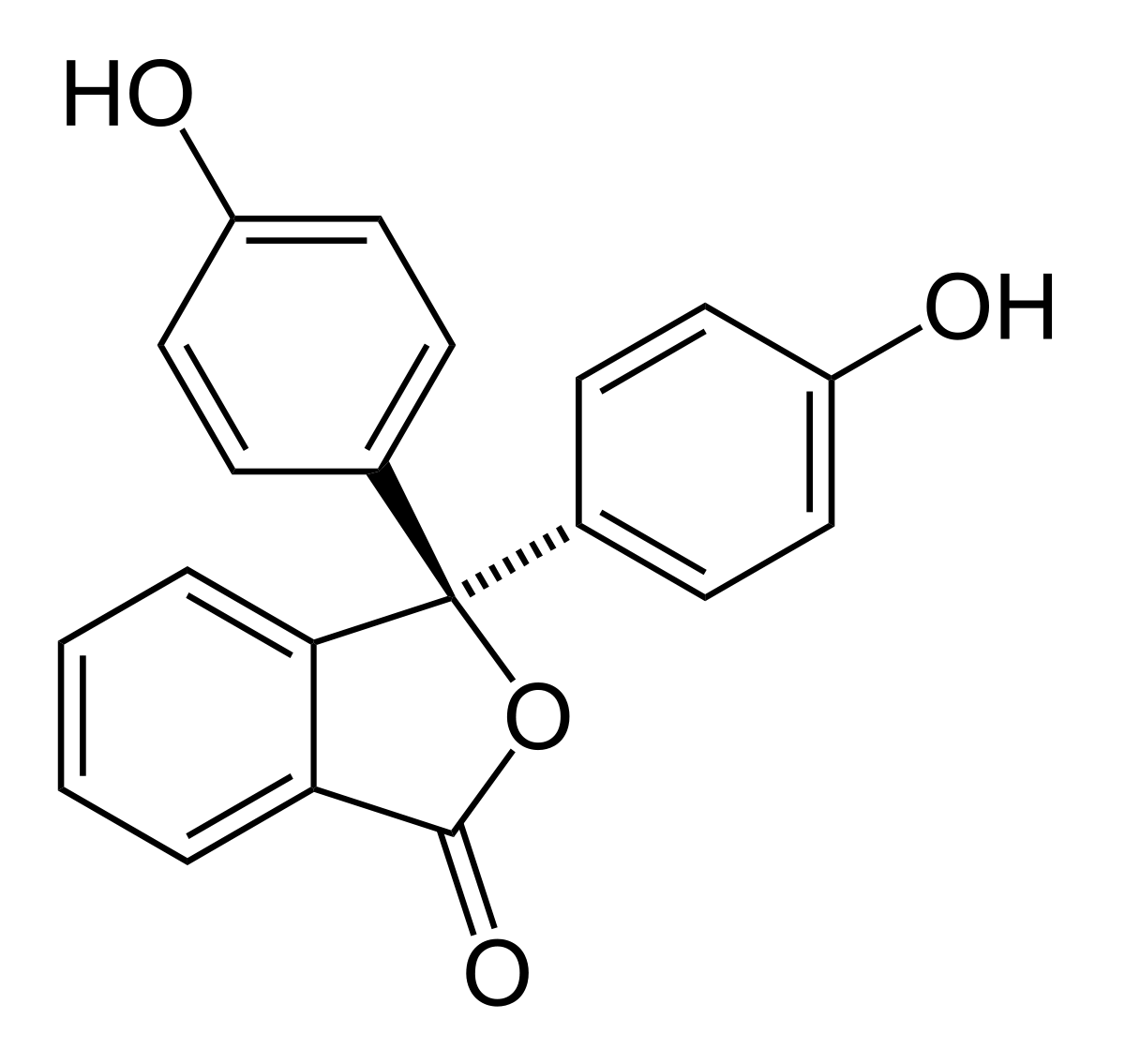
* Phân loại phenol:
- Loại monophenol: Đây là những phenol mà phân tử có chứa 1 nhóm -OH">OH. Ví dụ: phenol, o-crezol, m-crezol, p-crezol...
- Loại poliphenol: Là những phenol mà phân tử có chứa nhiều nhóm OH">OH.
Ví dụ:
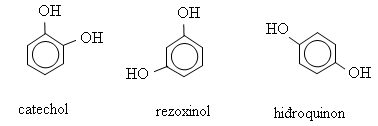
2. Tính chất của Phenol là gì?
* Tính chất vật lí:
- Phenol là chất tinh thể không màu, nóng chảy ở nhiệt độ 42oC.
- Ở nhiêt độ thường, phenol ít tan trong nước, khi đun nóng độ tan tăng lên. Khi đun nóng ở nhiệt độ 70oC trở lên thì tan vô hạn trong nước. Phenol tan nhiều trong rượu, ete, clorofom, …
- Phenol độc, có tính sát trùng, làm bỏng da.
* Tính chất hóa học:
- Phản ứng thế nguyên tử hiđro của nhóm OH
* Tác dụng với kim loại kiềm:
C6H5OH + Na → C6H5ONa (Natri phenolat) + 1/2 H2↑
* Tác dụng với bazơ:
C6H5OH (rắn, không tan) + NaOH → C6H5ONa (tan, trong suốt) + H2O
→ Phenol có tính axit, tính axit của phenol rất yếu; dung dịch phenol không làm đổi màu quỳ tím.
Chú ý: tính axit yếu, không làm đổi màu quỳ tím, thứ tự: nấc II của H2CO3 < phenol < nấc I của H2CO3.
⇒ Có phản ứng:
C6H5ONa (dd trong suốt) + H2O + CO2 → C6H5OH (vẩn đục) + NaHCO3
C6H5OH + Na2CO3 → C6H5ONa + NaHCO3
- Phản ứng thế nguyên tử hiđro của vòng benzene
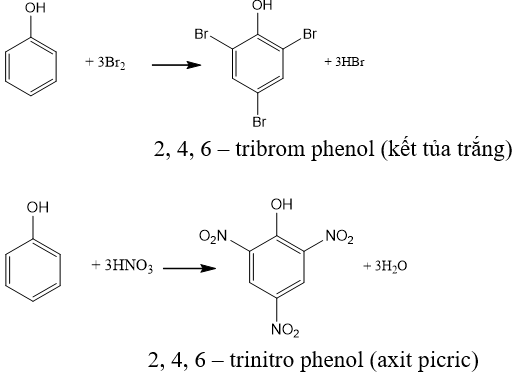
+ Phản ứng với H2:
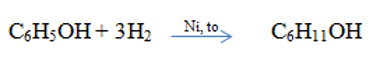
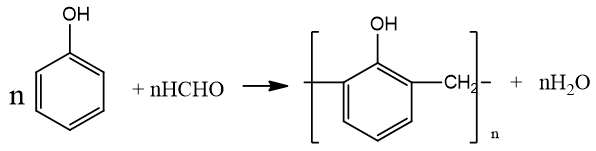
+ Phản ứng trùng ngưng với fomandehit:
3. Phenol là chất điện li mạnh hay yếu?
- Trong môi trường nước, Phenol là một chất điện li yếu. Mặc dù có khả năng phân li ra ion H+ (tạo tính axit) nhưng phenol chỉ phân li rất hạn chế trong dung dịch nước, do đó không làm đổi màu quỳ tím. Tính axit của phenol rất yếu, yếu hơn nhiều so với các axit vô cơ và thậm chí yếu hơn cả axit carbonic (H2CO3)
4. Phenol có làm mất màu dung dịch Brom không?
- Một trong những cách nhanh nhất để nhận biết Phenol chính là sử dụng dung dịch Brom. Phenol có khả năng làm mất màu dung dịch Brom và tạo ra kết tủa trắng tinh khiết ngay ở điều kiện thường.
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
↓ trắng
- Hiện tượng nhận biết phản ứng Phenol tác dụng với brom: Dung dịch Brom (Br2) bị mất màu, dần xuất hiện kết tủa trắng.
5. Cách điều chế Phenol
- Từ benzen:
+ Từ benzen, ta có thể điều chế ra hợp chất phenol qua các chuỗi phản ứng như sau:
C6H6 + Br2 -> C6H5Br+ HBr (xúc tác bột Fe)
C6H5Br + 2NaOH (đặc) -> C6H5ONa + NaBr + H2O (nhiệt độ và áp suất cao)
C6H5ONa + CO2 + H2O -> C6H5OH + NaHCO3
- Từ than đá:
+ Ta tiến hành cho nhựa than đá phản ứng với dung dịch NaOH lấy dư. Sau đó, từ từ tách chiết để lấy lớp nước có chứa C6H5ONa. Cuối cùng, cho C6H5ONa + H+ để thu được phenol.
- Điều chế phenol trong công nghiệp:
+ Trong công nghiệp, phenol sẽ được điều chế từ việc oxi hóa cumen (isopropylbenzen). Sản phẩm tạo ra sau khi thủy phân bằng loãng là hỗn hợp Phenol và Axeton. Bằng cách đun nóng, người ta tách được Axeton bay hơi và thu về Phenol nguyên chất.
6. Ứng dụng
- Phenol đã được ứng dụng rộng rãi trong nhiều lĩnh vực như:
+ Sản xuất các hợp chất ở dạng thơm như caprolactam, cyclohexanone, xylene
+ Điều chế thuốc trừ sâu, chất diệt khuẩn và thuốc nhuộm.
+ Sản xuất chất dẻo, chất nhựa cứng epoxy, poliamit, tơ nhân tạo
+ Sử dụng làm chất bảo quản, xử lý củi và vật liệu chèn gỗ bền bỉ.
+ Thành phần trong bột thơm, mỹ phẩm
