1. NaOH là gì?
- Sodium Hydroxide, hay còn được biết đến với công thức hóa học NaOH là một hợp chất vô cơ, một bazơ mạnh thuộc nhóm kiềm. Nó còn được biết đến rộng rãi với các tên gọi khác như Natri Hydroxit, Xút ăn da, Caustic Soda, hoặc kiềm nóng chảy. Đây là một hóa chất công nghiệp quan trọng, được sử dụng với số lượng lớn trên toàn cầu.
- Đặc điểm cấu tạo và công thức phân tử:
+ Về mặt cấu trúc, một phân tử NaOH được hình thành từ sự kết hợp giữa ion Natri () mang điện tích dương và ion Hydroxit () mang điện tích âm. Chúng gắn kết với nhau bằng liên kết ion bền vững. Sự tồn tại dưới dạng ion này là yếu tố chính quyết định tính chất hóa học đặc trưng của NaOH, đặc biệt là tính bazơ mạnh của nó trong dung dịch nước. Khi tan trong nước, các ion Na+ và OH− phân ly hoàn toàn, giải phóng ion OH− – tác nhân chính gây ra tính kiềm.
2. Tính chất của NaOH là gì?
- Tính chất vật lý:
+ NaOH có dạng rắn tinh thể màu trắng, dễ hút ẩm và tan rất tốt trong nước. Quá trình tan NaOH trong nước tạo ra nhiệt, dung dịch NaOH có khả năng làm thay đổi độ pH, từ đó tạo ra môi trường kiềm mạnh. Từ đó mà loại hóa chất này đóng vai trò như một chất tăng độ pH của nước hiệu quả.
- Tính chất hóa học: NaOH là một bazơ mạnh, có khả năng phản ứng với nhiều chất hóa học khác. Nó dễ dàng trung hòa axit để tạo ra muối và nước. Một số phản ứng phổ biến bao gồm:
+ Phản ứng với axit clohydric (HCl) để tạo ra muối natri clorua (NaCl) và nước: NaOH + HCl → NaCl + H2O
+ Phản ứng với kim loại như nhôm hoặc kẽm để tạo ra khí hydro (H2): Al + NaOH + H2O → NaAlO2 + H2 hoặc NaOH + Zn → Na2ZnO2 + H2
- Tính ăn mòn: NaOH có khả năng ăn mòn kim loại, vải và nhiều vật liệu khác, vì vậy cần được xử lý cẩn thận và sử dụng các biện pháp bảo hộ khi tiếp xúc trực tiếp.
- Độ pH: Độ pH của NaOH khoảng 13.5, thể hiện tính kiềm rất mạnh. Nhờ đó, NaOH được dùng để trung hòa axit và tạo môi trường kiềm trong nhiều quy trình hóa học như sản xuất xà phòng, chất tẩy rửa hoặc xử lý nước.
3. NaOH điện li mạnh hay yếu?
- NaOH (Natri hydroxit) là một chất điện li mạnh. Khi tan trong nước, NaOH phân li hoàn toàn thành các ion Na+ và OH-, tạo ra dung dịch có khả năng dẫn điện mạnh. Là một bazơ mạnh, NaOH phân li gần như 100% trong dung dịch.
* Phương trình điện li:
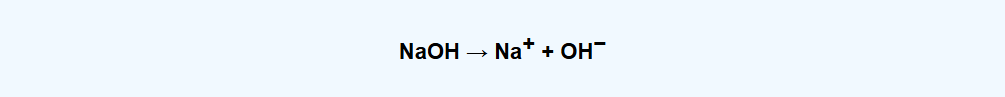
4. Ứng dụng của NaOH
- Ngành giấy: Dùng để xử lý các nguyên liệu thô như tre, nứa, gỗ... giải phóng sợi xenluloza để tạo nên những trang giấy ta dùng hàng ngày.
- Sản xuất hóa mỹ phẩm: Phân hủy chất béo trong dầu mỡ động thực vật để tạo ra xà phòng và các chất tẩy rửa.
- Chế biến thực phẩm: Đóng vai trò tinh chế dầu ăn, giúp loại bỏ các axit béo tự do trước khi thành phẩm đến tay người tiêu dùng.
- Luyện kim và Năng lượng: Làm sạch quặng nhôm trước khi đưa vào sản xuất và hỗ trợ trong quy trình chế biến dầu mỏ.
- Xử lý môi trường: Điều chỉnh nồng độ pH trong công nghiệp hóa chất, đồng thời trung hòa và khử cặn bẩn trong các hệ thống đường ống cấp nước.
5. Cách điều chế NaOH
- Phương pháp phổ biến nhất để tạo ra NaOH là điện phân dung dịch nước muối có màng ngăn (còn gọi là quy trình Chloralkali).
- Việc xử lý điện phân nước muối để sản xuất Natri Hydroxit, clo và hydro được gọi là quá trình điện phân hay Chloralkali.Trong quá trình điện phân này, dung dịch muối (NaCl) được điện phân thành nguyên tố clo, dung dịch natri hydroxit và nguyên tố hydro. Nhà máy có thiết bị để sản xuất đồng thời cả Natri Hydroxit và clo thường được gọi là nhà máy xút - clo.
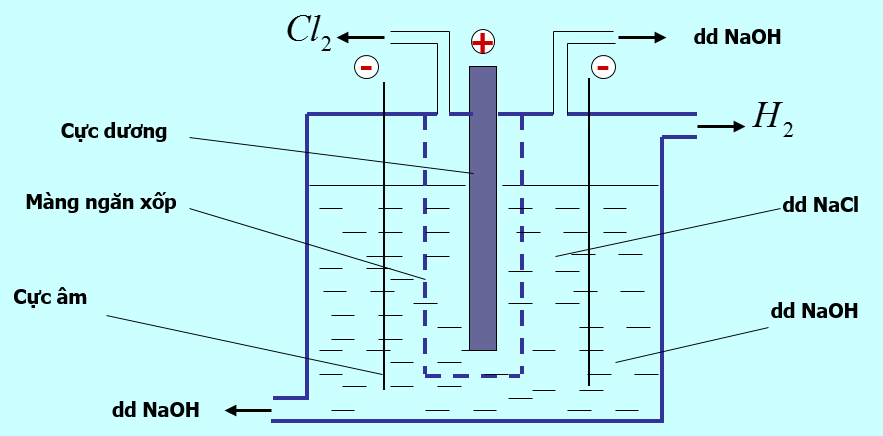
Phản ứng tổng thể để sản xuất Natri Hydroxit và clo bằng phương pháp điện phân là:
2 Na+ + 2 H2O + 2 e- → H2 + NaOH
Phản ứng điện phân dung dịch muối ăn trong bình điện phân muối có màng ngăn:
NaCl + 2 H2O → 2 NaOH + H2 + Cl2
