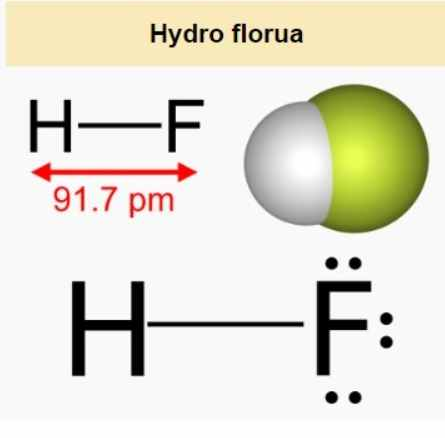
1. Flohydric acid (HF) là axit gì?
- Axit flohidric, Hydro florua là tên gọi chung của hóa chất có công thức hóa học là HF. Đây là một nguồn giá quý và là nguyên liệu sản xuất nhiều loại dược phẩm trong y tế. Trong hóa học, axit này được biết đến với khả năng hòa tan kính của nó khi hoạt động với SiO2.
- Trong môi trường tự nhiên, HF tồn tại ở dạng dư và dạng khí với mùi khó khó chịu. Ở dạng dịch HF được gọi là axit flohydric. Cho đến nay, hóa chất HF đang được sử dụng rộng rãi trong các ngành công nghiệp hóa dầu cùng các ngành công nghiệp khác.
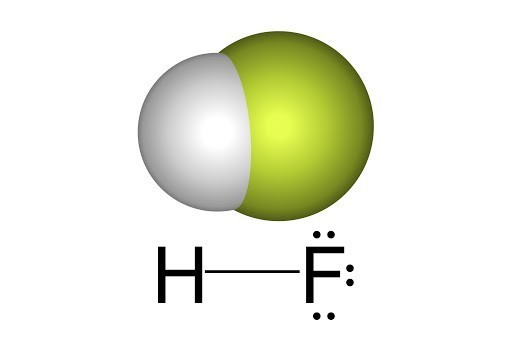
2. Flohydric acid (HF) có những tính chất gì?
a. Tính chất vật lý
- Khối lượng riêng: 1.15 g/L, gas (25°C); 0.99 g/mL, liquid (19.5°C)
- Điểm nóng chảy: −83,6°C (189,6 K; −118,5°F)
- Điểm sôi: 19,5°C (292,6 K; 67,1°F)
- Áp suất hơi: 783 mmHg (20°C)
- Độ axit (pKa): 3.17
- Độ hòa tan trong nước: >95%
- Phân tử khối nhẹ hơn không khí.
b. Tính chất hóa học
- Tác dụng với phi kim:
O2 + HF → HFO2
I2 + HF → HFI4
2Br2 + HF → HFBr4
- Tác dụng với oxit:
SiO2 + 4HF → 2H2O + SiF4
SO3 + HF → HSO3F
- Tác dụng với nước:
2H2O + HF → 2H2 + HFO2
H2O + HF + AsF5 → HAsF6.H2O
- Tác dụng với bazơ
NaOH + HF → H2O + NaF
Ca(OH)2 + 2HF→ CaF2 + 2H2O
- Tác dụng với muối
NaF + HF ↔ NaHF2
CuCl + HF→ HCl+CuF
3. Axit hydrofluoric (HF) là axit mạnh hay axit yếu?
- Axit flohydric (HF) được phân loại là axit yếu. Mặc dù HF rất ăn mòn, nhưng nó không được coi là axit mạnh. Bởi vì liên kết giữa H và F rất bền nên HF không phân ly nhiều trong nước. Trong khi đó, vì sự phân ly hoàn toàn là đặc điểm chính của axit mạnh, nên HF được coi là axit yếu.
4. Cách nhận biết Axit flohiđric
- Axit flohiđric là một axit yếu.
- Cách nhận biết: Dùng quỳ tím
- Hiện tượng: Quỳ tím hóa đỏ nhạt.
Lưu ý:
- Không dùng AgNO3 nhận biết HF vì không có phản ứng xảy ra.
- Khi nhận biết các đồng thời dung dịch axit HF, HCl, HBr, HI thì dùng dung dịch AgNO3, hiện tượng:
+ Không hiện tượng: HF
+ Xuất hiện kết tủa trắng: HCl
AgNO3 + HCl → AgCl↓ + HNO3
+ Xuất hiện kết tủa màu vàng nhạt: HBr
AgNO3 + HBr → AgBr↓ + HNO3
+ Xuất hiện kết tủa màu vàng đậm: HI
AgNO3 + HI→ AgI↓ + HNO3

5. Ứng dụng Axit hydrofluoric (HF)
- Khắc và xử lý kính
+ Một trong những ứng dụng nổi bật nhất của HF là khắc chữ, tạo hoa văn trên thủy tinh và pha lê. HF có khả năng hòa tan SiO₂ – thành phần chính của kính, giúp bề mặt kính trở nên mờ hoặc được tạo hình nghệ thuật theo mong muốn. Nhờ đó, HF được ứng dụng rộng rãi trong:
- Sản xuất kính trang trí, kính mờ.
+ Khắc logo hoặc họa tiết trên ly, cốc, chai lọ thủy tinh.
+ Xử lý bề mặt quang học trong sản xuất thiết bị đo lường.
- Tẩy rửa và xử lý bề mặt kim loại
+ Axit Flohydric được sử dụng trong quá trình tẩy rửa thiết bị công nghiệp, đặc biệt là trong các ngành:
+ Cơ khí – luyện kim: Loại bỏ oxit kim loại (gỉ sét) trên thép, inox trước khi hàn hoặc mạ.
+ Ngành năng lượng: Tẩy cáu cặn trong các thiết bị trao đổi nhiệt, nồi hơi và ống dẫn công nghiệp.
+ Công nghiệp hóa chất: Tẩy rửa bồn chứa, bồn phản ứng, thiết bị gia công kim loại sau quá trình vận hành lâu dài.
- Sản xuất hợp chất chứa flo
HF là nguyên liệu chính để sản xuất nhiều hợp chất flo quan trọng, bao gồm:
+ Polymer flo hóa: Đặc biệt là Teflon (PTFE) – vật liệu chống dính, chịu nhiệt, cách điện tốt.
+ Hóa chất dược phẩm: Tổng hợp các hợp chất hữu cơ chứa flo trong các loại thuốc điều trị.
+ Chất làm lạnh và chất chống cháy: Là tiền chất để sản xuất các hợp chất flo hóa như HFCs, HCFCs.
- Ứng dụng trong dầu khí
+ Trong ngành lọc hóa dầu, HF đóng vai trò là chất xúc tác trong quá trình ankyl hóa, giúp sản xuất ra xăng có chỉ số octane cao hơn. Điều này giúp:
+ Nâng cao hiệu suất động cơ.
+ Giảm khí thải độc hại ra môi trường.
+ Tối ưu hóa quy trình sản xuất nhiên liệu sạch cho ngành công nghiệp năng lượng.
+ Axit Flohydric không chỉ là hóa chất chuyên dụng trong phòng thí nghiệm mà còn giữ vai trò quan trọng trong nhiều ngành công nghiệp như: thủy tinh, cơ khí, hóa chất, dầu khí và sản xuất các sản phẩm công nghệ cao.
6. Cách điều chế Axit hydrofluoric (HF)
- Để điều chế HF, người ta dùng phương pháp sunfat. Đó là cho H2SO4 đặc tác dụng với muối florua, clorua vì H2SO4 là chất oxi hoá không đủ mạnh để oxi hoá được HF. Hay nói cách khác là HF có tính khử yếu, chúng không khử được H2SO4 đặc
- Phương trình hóa học điều chế HF:
CaF2 + H2SO4 → CaSO4 + 2HF
- Điều kiện phản ứng: Nhiệt độ 2500C
- Cách thực hiện phản ứng: Cho florit tác dụng với dung dịch H2SO4 đặc.
- Hiện tượng nhận biết: Có khí thoát ra.
=> Đây là cách duy nhất để điều chế HF.