1. Aluminum là gì?
- Aluminum hay còn gọi là nhôm, là một nguyên tố hóa học có ký hiệu Al, thuộc nhóm kim loại nhẹ trong bảng tuần hoàn. Với sắc trắng bạc đặc trưng, nhôm nổi tiếng nhờ đặc tính mềm, dẻo, khả năng dẫn điện và nhiệt vượt trội. Đặc biệt, nhôm sở hữu khả năng tự bảo vệ mình trước sự ăn mòn của môi trường nhờ một lớp oxit tự nhiên siêu mỏng nhưng cực kỳ bền vững bao phủ trên bề mặt.
- Trong thực tế, nhôm có nhiều tên gọi khác nhau như alumi, nhôm aluminum hay dưới dạng vật liệu cụ thể là chất liệu alu, vật liệu alu. Đặc biệt, alu là tấm hợp kim nhôm – nhựa có trọng lượng nhẹ, bền đẹp, thường dùng trong xây dựng và nội thất.
- Ngoài nhôm nguyên chất còn có aluminum alloy – hợp kim nhôm được pha trộn thêm các nguyên tố như đồng, magie, mangan hoặc kẽm để tăng độ cứng, độ bền và khả năng chịu lực. Nhờ đó, chất liệu aluminum đáp ứng tốt cả nhu cầu dân dụng lẫn công nghiệp.
2. Aluminum có những tính chất gì?
* Tính chất vật lí:
- Trọng lượng: Chỉ khoảng 2.7 g/cm3, Nhôm cực kỳ nhẹ – nhẹ hơn sắt và đồng đáng kể, lý tưởng cho các ứng dụng cần giảm trọng lượng.
- Độ ổn định cao: Nhôm có điểm nóng chảy tương đối thấp (660.3∘C) (thuận tiện cho việc đúc, gia công) nhưng chỉ sôi ở mức 2519°C, đảm bảo sự ổn định trong nhiều môi trường nhiệt độ.
- Dẫn điện và nhiệt: dẫn điện và dẫn nhiệt rất tốt, có khả năng phản xạ ánh sáng và nhiệt cao.
- Không từ tính: Một ưu điểm quan trọng cho các thiết bị điện tử và ứng dụng chuyên dụng.
* Tính chất hóa học:
- Nhôm là kim loại có tính khử mạnh, dễ dàng nhường electron trong các phản ứng hóa học.
- Điểm đặc biệt của Nhôm là khả năng tạo thành lớp màng oxit mỏng (Al2O3) bền vững ngay khi tiếp xúc với không khí. Lớp màng này đóng vai trò như một lớp áo giáp, bảo vệ Nhôm khỏi quá trình oxy hóa tiếp theo và sự ăn mòn, khiến nó trở nên rất bền trong môi trường tự nhiên.
- Dù có tính khử mạnh, Nhôm thể hiện tính chất lưỡng tính độc đáo khi phản ứng. Nó có thể tác dụng với cả axit mạnh (không phải axit oxy hóa mạnh như HNO3 đặc nguội) và bazơ mạnh:
+ Phản ứng với axit: 2Al + 6HCl → 2AlCl3 + 3H2↑
+ Phản ứng với bazơ: 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑ (hoặc 2Na[Al(OH)4])
- Bên cạnh đó, Nhôm còn dễ dàng phản ứng với các phi kim như Oxy để tạo thành oxit Nhôm. Điều này cũng dẫn đến việc Oxit Nhôm (Al2O3) và Hydroxit Nhôm (Al(OH)3) đều có tính lưỡng tính, tức là chúng có thể phản ứng với cả axit và bazơ, một đặc điểm hóa học quan trọng của Nhôm.
3. Ứng dụng của Aluminum trong thực tế
- Kiến trúc và Quảng cáo: Là vật liệu chính làm biển hiệu, trang trí mặt tiền cao ốc và thiết kế nội thất nhờ khả năng cách âm, chống cháy và vẻ ngoài thẩm mỹ.
- Công nghiệp vận tải và Năng lượng: Chế tạo thân vỏ xe máy, đóng tàu, vỏ máy bay và là lõi của các dây dẫn điện cao thế.
- Ngành Thực phẩm và Y tế: Nhôm hoàn toàn không độc hại ngay cả khi cơ thể hấp thụ một lượng nhỏ. Vì vậy, nó được dùng làm màng bọc thực phẩm, xoong nồi, thiết bị y tế và đặc biệt là vỏ lon nước giải khát (như Coca-Cola) với khả năng tái chế 100%.
- Chế tạo máy: Các loại hợp kim nhôm với tỉ lệ 1% các nguyên tố như silicon, kẽm, magie... giúp tăng cường độ cứng đáng kể nhưng vẫn giữ được ưu điểm nhẹ và không bị gỉ sét.
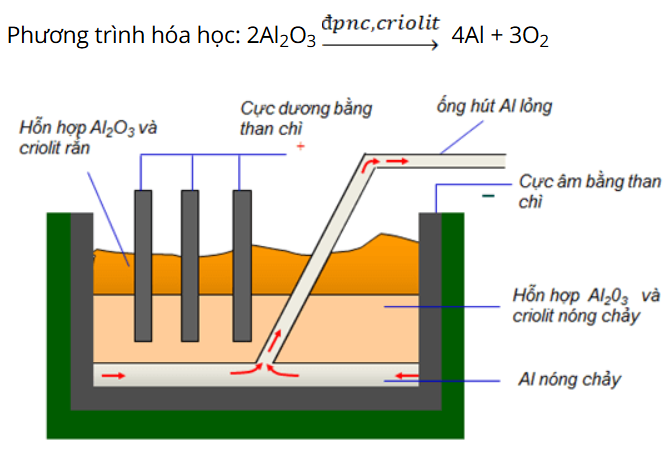
4. Cách điều chế Aluminum
- Trong tự nhiên, Al tồn tại dưới dạng oxit, muối. Để sản xuất nhôm, người ta sử dụng nguyên liệu chính là quặng boxit, có thành phần chính là Al2O3.
- Quặng boxit sau khi được làm sạch tạp chất, sau đó điện phân nóng chảy hỗn hợp Al2O3 và criolit (chất làm giảm to nóng chảy của Al) trong bể điện phân.