1. Kim loại là chất gì?
- Kim loại là tập hợp các nguyên tố có thể tạo ra các ion dương (cation) và có các loại kim liên kết. Cùng với phi kim và á kim, các loại kim cũng được phân biệt bởi mức độ ion hóa. Trong bảng tuần hoàn hóa học, chiếm tới 80% tổng số nguyên tố, trong khi đó cả kim và phi kim chỉ sử dụng 20%.
- Kim loại tồn tại dưới nhiều hình thái đa dạng: có thể là một nguyên tố nguyên chất như Sắt (Fe), một hợp kim bền bỉ như thép không gỉ, hay thậm chí là những hợp chất phân tử độc đáo như polyme lưu huỳnh nitrit.
2. Đặc điểm và cấu tạo của kim loại là gì?
a. Đặc điểm cấu tạo
- Kim loại có tính chất khác nhau là do tổ chức bên trong của chúng khác nhau. Vật chất do các nguyên tử tạo thành;
- Mỗi nguyên tử là một hệ thống phức tạp bao gồm hạt nhân (có chứa notron, proton,…) và các lớp điện tử bao quanh nó 9điện tử có điện tích âm). Đối với kim loại thường quan tâm đến lớp điện tử ngoài cùng vì lớp bên trong rất bền vững;
- Đặc điểm quan trọng nhất về cấu tạo nguyên tử của kim loại là số điện tử hóa trị. Số điện tử ngoài cùng đối với kim loại thông thường và ở lóp sát ngoài đối với kim loại chuyển tiếp. Thông thường, các nguyên tố này chỉ có rất ít electron hóa trị (từ 1 đến 2). Do liên kết với hạt nhân khá lỏng lẻo, những electron này dễ dàng tách ra để trở thành các điện tử tự do, biến nguyên tử trung hòa thành ion dương.
b. Cấu tạo kim loại
- Cấu tạo tinh thể: Ngoại trừ Thủy ngân (Hg) tồn tại ở dạng lỏng, hầu hết kim loại ở điều kiện thường đều ở thể rắn với cấu trúc tinh thể chặt chẽ. Hạt nhân liên kết rất kém với các electron hóa trị do đó dễ tách khỏi nguyên tử và các electron di chuyển tự do trong mạng tinh thể kim loại. Mạng tinh thể kim loại gồm: lập phương tâm diện (CU, Au, Ag,…); lục phương (Mg, Be, Zn,…); lập phương tâm khối (Na, K, Li,…).
- Cấu tạo nguyên tử: nguyên tử của đa số các nguyên tố kim loại có rất ít electron ở lớp ngoài cùng (chỉ có 1, 2 hoặc 3 electron)
Ví dụ: Mg: 1s2 2s2 2p6 3s2
3. Tính chất của kim loại là gì?
a. Tính chất vật lí
- Cảm quan: Thường tồn tại ở thể rắn có ánh kim, đa dạng về màu sắc. Tuy nhiên, có một số trường hợp ngoại lệ như thủy ngân (Hg) và Copernixi (Cn) ở dạng lỏng.
- Khối lượng riêng tương đối lớn:
+ Kim loại nhẹ < 5g/cm³.
+ Kim loại trung bình < 10 g/cm³.
+ Kim loại nặng > 10g/cm³.
- Nhiệt độ nóng chảy thường cao.
- Có khả năng dẫn nhiệt và dẫn điện tốt.
- Cứng nhưng dễ kéo dài và dát mỏng.
- Nguyên tử kim loại không nhận thêm electron nên nó chỉ trở thành ion dương.
- Trong tự nhiên, rất ít kim loại tồn tại dưới dạng tự do (vàng, platin,...), chủ yếu là tồn tại dưới dạng hợp chất.
b. Tính chất hóa học
- Tác dụng với oxi:
+Phần lớn các kim loại hoạt động hóa học khá mạnh, phản ứng với oxi trong không khí để tạo thành oxit sau một khoảng thời gian khác nhau (ví dụ như sắt bị rỉ suốt mấy năm nhưng kali bùng cháy chỉ trong vài giây). Kim loại kiềm phải ứng mãnh liệt nhất, kế tiếp là kim loại kiềm thổ. Ví dụ:
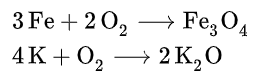
- Tác dụng với phi kim
+ Khi tiếp xúc với các halogen hoặc lưu huỳnh, kim loại sẽ chuyển hóa thành các dạng muối tương ứng (như muối sulfide), thường đẩy số oxy hóa lên mức cao đối với các kim loại đa hóa trị.
+ Ví dụ :
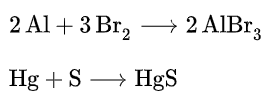
- Tác dụng với acid
+ Điều kiện: Các kim loại đứng trước Hidro trong dãy hoạt động hóa học sẽ dễ dàng phản ứng với acid để giải phóng khí và tạo muối.
+ Ví dụ :
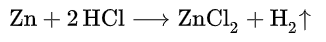
4. Kim loại được điều chế theo phương pháp nào?
a. Phương pháp thuỷ luyện
- Nguyên tắc: Dùng dung dịch hóa chất (như , ) để hòa tan kim loại từ quặng, sau đó dùng các chất khử mạnh như Fe, Zn để đẩy ion kim loại ra ngoài.
- Phạm vi áp dụng: Thường sử dụng để điều chế các kim loại có tính khử yếu (như Cu).
+ Ví dụ:
Fe + CuSO4 → FeSO4 + Cu↓
Fe + Cu2+ → Fe2+ + Cu↓
b. Phương pháp nhiệt luyện
- Nguyên tắc: Khử ion kim loại trong hợp chất ở nhiệt độ cao bằng các chất khử như C, CO, H2 hoặc các kim loại hoạt động.
- Phạm vi áp dụng: Sản xuất các kim loại có tính khử trung bình (Zn, FE, Sn, Pb, …) trong công nghiệp.
+ Ví dụ:
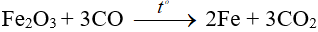
c. Phương pháp điện phân
* Điện phân hợp chất nóng chảy
- Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân nóng chảy hợp chất của kim loại.
- Phạm vi áp dụng: Điều chế các kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al.
+ Ví dụ: Điện phân MgCl2 nóng chảy để điều chế Mg.
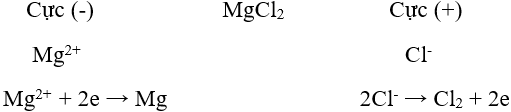
Phương trình điện phân:
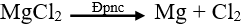
* Điện phân dung dịch
- Nguyên tắc: Điện phân dung dịch muối của kim loại.
- Phạm vi áp dụng: Áp dụng cho các kim loại có độ hoạt động trung bình hoặc yếu.
+ Ví dụ: Điện phân dung dịch CuCl2 để điều chế kim loại Cu.
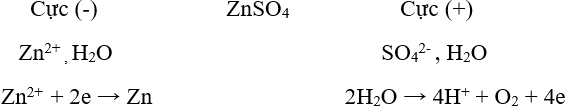
Phương trình điện phân:
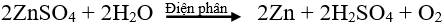
5. Ứng dụng của kim loại trong đời sống hiện nay
- Trong sản xuất:
+ Kim loại được dụng nhiều trong ngành luyện kim và sản xuất, gia công cơ khí, chế tạo máy móc, thiết bị. Sắt, thép (và hợp kim của chúng như inox) hoặc nhôm, kẽm. Là nguyên liệu cốt lõi để chế tạo máy móc, khuôn đúc và các chi tiết cơ khí chính xác.
- Trong xây dựng:
+ Kim loại đen, kim loại cơ bản thường được dùng để phục vụ cho các công trình xây dựng như nhà ở, tòa nhà, cầu đường, các kiến trúc lớn nhỏ khác nhau…Tạo nên khung xương vững chắc cho các tòa cao ốc, cầu đường và các kiến trúc.
- Trong giao thông vận tải:
+ Ứng dụng làm vỏ các loại phương tiện, chi tiết máy móc, thiết bị và phụ kiện, khớp nối trong hầu hết các phương tiện từ xe đạp, xe máy, ô tô, xe tải, máy bay hay tàu thủy.
- Trong gia dụng:
+ Kim loại được sử dụng để tạo ra các sản phẩm phục vụ đời sống như bàn ghế, dụng cụ bếp, cầu thang, cửa, cổng…
- Trang trí – thiết kế:
+ Ngoài ra, kim loại màu như còn được dùng nhiều trong trang trí nội thất nhờ khả năng uốn lượn, tạo hình đầy nghệ thuật. Giúp sản phẩm vừa mang tính ứng dụng thực tiễn, vừa làm đẹp cho không gian.
- Trong hóa học:
+ Đóng vai trò là chất xúc tác và đối tượng phân tích trong các phòng thí nghiệm, giúp con người tìm ra những vật liệu mới ưu việt hơn.
