1. H2SO3 là gì?
- H2SO3 (axit sunfurơ) là một axit yếu và có khả năng phân ly trong nước thành các ion, nhưng quá trình này chỉ xảy ra một phần, không hoàn toàn như các axit mạnh.
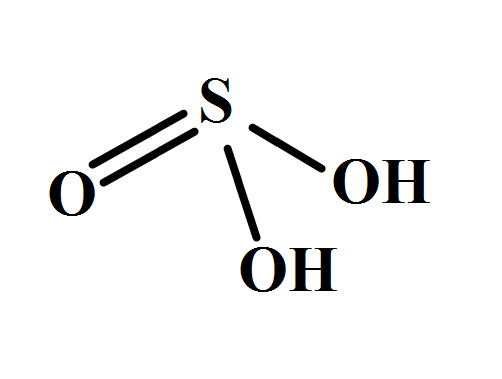
- H2SO3 có cấu trúc gồm một nguyên tử lưu huỳnh (S) liên kết với ba nguyên tử oxy (O) và hai nguyên tử hydro (H). Khi tan trong nước, H2SO3 phân ly qua hai giai đoạn:
+ Giai đoạn 1: H2SO3 ⇌ H+ + H2SO3-
+ Giai đoạn 2: H2SO3- ⇌ H+ + SO32-
2. H2SO3 có tính chất gì?
a. Tính chất vật lí:
- H2SO3 không màu, trong suốt như nước. Ở điều kiện thường, H2SO3 chủ yếu tồn tại ở dạng dung dịch lỏng. Điểm đặc biệt của hợp chất này là chúng ta không thể tách ra khỏi nước để thu được chất tinh khiết, bởi H2SO3 dễ bị phân hủy thành SO2 và H2O.
- Dung dịch H2SO3 thường có mùi hắc, xốc (quyết định bởi khí lưu huỳnh đioxit). Khi hít trực tiếp, cơ thể dễ bị kích ứng.
- H2SO3 chính là sản phẩm của quá trình hòa tan khí SO2 trong nước. Tuy nhiên ngay khi được tạo thành, hợp chất này có xu hướng bị phân hủy thành SO2 và H2O.
b. Tính chất hóa học:
* Tính axit yếu
- H2SO3 được xếp vào nhóm axit yếu nhưng có hằng số phân li nấc 1 khá lớn. Nhờ đó, loại axit này có khả năng phân li tạo ion H+ vừa đủ để thể hiện một số tính chất axit đặc trưng như:
+ Tác dụng với kim loại: H2SO3 có xu hướng tác dụng với kim loại đứng trước Hidro như Mg, Zn, Al, từ đó giải phóng khí H2.
+ Tác dụng với muối của axit yếu hơn: H2SO3 có khả năng đẩy CO2 ra khỏi Na2CO3 (H2SO3 + Na2CO3 → Na2SO3 + H2O + CO2).
* Tính khử
- Số oxi hóa của S trong H2SO3 là +4 (chưa bền), nguyên tử S thường có xu hướng nhường 2e để đạt số oxi hóa cao nhất là +6.
- Khi H2SO3 tác dụng với một số hợp chất hữu cơ tạo màu, nó có khả năng khử liên kết đôi thành liên kết đơn. Với tính khử, H2SO3 có thể tham gia phản ứng với các chất oxi hóa yếu hoặc trung bình ngay trong điều kiện thường. Ví dụ như khi tác dụng với muối sắt (III):
H2SO3 + 2FeCl3 + H2O → 2FeCl2 + H2SO4 + 2HCl
- Hiện tượng của phản ứng trên là dung dịch màu vàng nâu nhạt dần. Nhờ tính khử đặc trưng, H2SO3 có thể được ứng dụng để loại bỏ tạp chất oxi hóa trong quy trình sản xuất thực phẩm hoặc dược phẩm.
* Tính oxi hóa
- Khi tác dụng với các chất có khả năng nhường electron mạnh, H2SO3 thường đóng vai trò như chất oxi hóa. Cụ thể, S(+4) có xu hướng nhận thêm electron để giảm xuống 0 hoặc -2.
- Khi tác dụng với H2S: H2SO3 + 2H2S → 3S (kết tủa vàng) + 3H2O
- Khi tác dụng với kim loại mạnh: H2SO3 có thể oxi hóa nhiều kim loại mạnh như Magie.
* Tính chất tẩy màu
- H2SO3 có khả năng tẩy màu của một số hợp chất. Tuy nhiên không giống như Cl2 tẩy màu theo cơ chế phá hủy, H2SO3 thường được phối hợp cùng một số hợp chất hữu cơ khác để tạo ra hợp chất không màu mới. Đây là dạng phản ứng không bền. Theo đó khi nung nóng hoặc tiếp xúc lâu với không khí, hợp chất không màu dễ bị phân hủy, giải phóng sắc tố ban đầu.
3. H2SO3 là chất điện li mạnh hay yếu?
- H2SO3 là chất điện li yếu.
- H2SO3 là một axit yếu. Trong dung dịch H2SO3 sẽ phân li thuận nghịch theo 2 nấc.
- Các axit yếu, bazơ yếu và một số muối là chất điện li yếu.
- Các axit yếu như CH3COOH, H3PO4, HClO, H2S, HF, H2SO3, ...
4. Một số ứng dụng của H2SO3
* Trong ngành công nghiệp:
- Axit H2SO3 được sử dụng trong quá trình sản xuất sulfites, một loại chất bảo quản thực phẩm, bia và rượu với vai trò ngăn chặn quá trình oxy hóa và làm tăng tuổi thọ của sản phẩm.
- Nó được sử dụng làm chất khử trong quá trình sản xuất giấy để loại bỏ lignin, một chất gây màu và độc hại được tìm thấy trong cây gỗ.
- Axit H2SO3 cũng được sử dụng làm chất oxi hóa trong quá trình tổng hợp một số dẫn xuất hữu cơ, như axit ascorbic trong quá trình sản xuất Vitamin C.
* Trong khảo cổ học:
- Axit H2SO3 được sử dụng làm chất chống oxy hóa trong quá trình tạo đồng nhất của các mảnh vỡ thuộc văn hóa cổ. Bằng cách chống oxi hóa, axit H2SO3 giúp bảo quản và bảo vệ các mảnh vỡ khỏi quá trình mục nát và phá hủy.
- Nó cũng được sử dụng để làm sạch các vật liệu khác nhau, như kim loại và gốm sứ, bằng cách loại bỏ các tạp chất và mảng bám trên bề mặt.
